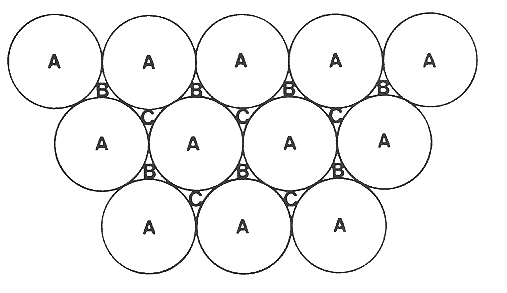
Periodické uspořádání stejně velkých atomů v prostoru je možné provést dvěma způsoby. Vyjdeme z hexagonálního netěsnějšího uspořádání atomů v ploše, které vytváří vrstvu (síť) s hexagonální symetrií. Mezi atomy lze rozlišit dva typy dutin, která mají v ploše tvar trojúhelníku a mají různou orientaci. Druhou vrstvu stejně uspořádaných atomů uložíme nad jeden typ intersticiál vrstvy první, což je s ohledem na volnou energii atomů nejvýhodnější. V případě, že třetí vrstvu atomů položíme do stejné pozice jako byla vrstva první, vznikne dvojvrstevný sled ABAB…. Tento typ struktury se označuje jako hexagonální nejtěsnější uspořádání nebo hcp struktura (z angličtiny hexagonal close-packed structure).

Dva typy intersticiál, které vzniknou mezi stejně velkými atomy uspořádanými do vrstvy s hexagonální symetrií.
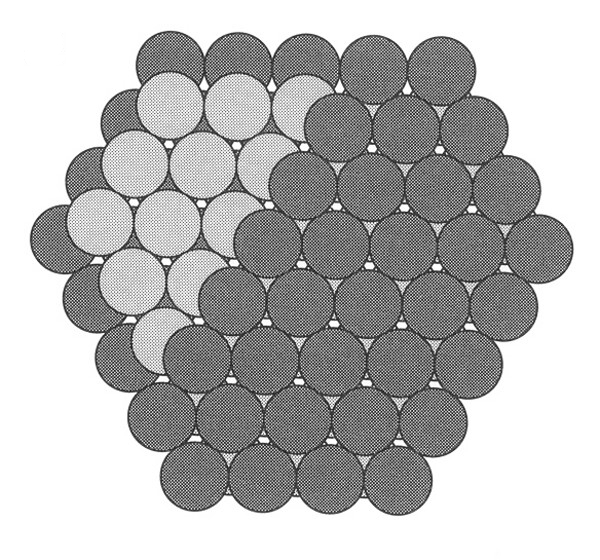
Dvojvrstevný sled ABAB nejtěsnějšího uspořádání stejně velkých atomů.
Stejně velké atomy v tomto uspořádání vyplní prostor ze 74 %, zbytek připadá na intersticiály. Každý atom je obklopen šesti atomy ve stejné vrstvě, třemi atomy z vrstvy spodní a třemi atomy z vrstvy horní. Výsledkem je 12-ti četná koordinace každého atomu.
Klad vrstev je kolmý k šestičetné ose, která je jedním z prvků symetrie této struktury. Ve směru šestičetné osy také probíhá souvislý kanál z intersticiál (dutiny typu C), které by v ccp struktuře obsadily atomy vrstvy C (viz struktura ccp).